全程導醫網 徐州行業動態:徐州市一院醫學倫理委員會在科教處辦公區會議室召開第三季度倫理審查會議,對市一院11項臨床研究項目進行倫理快速審查和倫理會議審查。醫學倫理委員會成員、項目負責人及相關人員按照疫情防控要求出席本次會議。市一院醫學倫理委員會主任趙玉良主持會議。

1)快速審查
主任委員趙玉良、主審委員李泳對市一院近期獲得的江蘇大學2021年臨床醫學科技發展基金(自然科學類)項目中涉及人的4項臨床研究項目和市一院消化內科主任陳光俠開展的藥物臨床III期項目《甲磺酸帕拉德福韋片治療慢性乙型肝炎的隨機、雙盲、陽性藥平行對照、多中心、III期臨床試驗》遞交的修正案審查項目進行倫理快速審查。
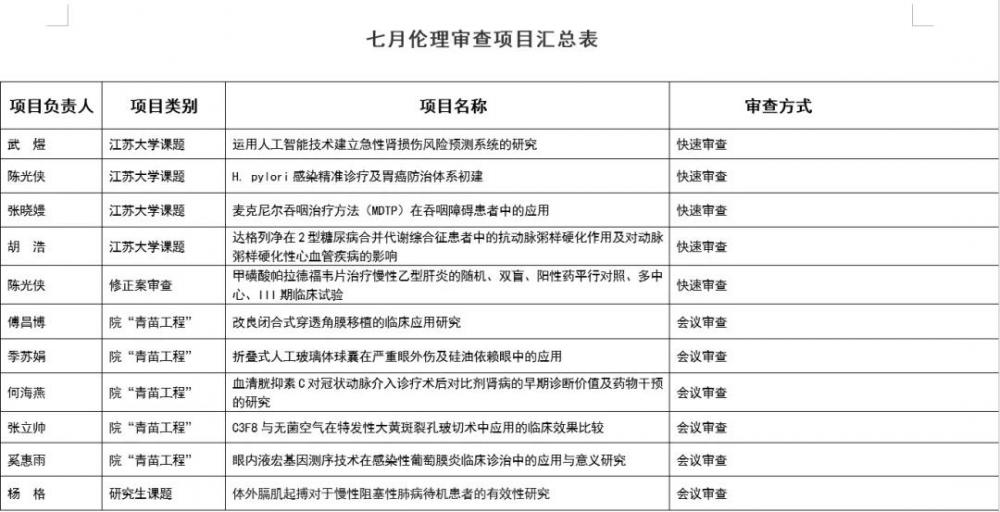
2)會議審查
醫學倫理委員會在第三階梯教室對市一院“青苗工程”課題中涉及器官移植、高風險手術、并發癥較多、涉及倫理問題的5個項目和1項研究生課題進行倫理會議審查。趙玉良主持會議,市一院醫學倫理委員、外院律師、社區人士、獨立技術顧問參加會議,人數超過半數,符合法定要求。涉及的項目負責人進行了PPT匯報和答辯,委員們集體商議后投票表決,同意超過半數的項目,醫學倫理委員會下達批件。



倫理知識科普
《涉及人的生物醫學研究倫理審查辦法》(11號令)
2007年原衛生部發布了《涉及人的生物醫學研究倫理審查辦法(試行)》(以下簡稱《辦法(試行)》)。該審查辦法對宣傳普及科研倫理原則,建立健全受試者保護機制,規范生物醫學研究行為起到了積極促進作用,但隨著生物醫學研究的快速發展和倫理審查工作的逐步深入,《辦法》(試行)作為規范性文件已不能滿足發展需要,迫切需要根據當前臨床研究管理工作要求,統籌規劃制度建設,進一步細化倫理審查、知情同意內容和規程,加強涉及人的生物醫學研究倫理審查工作的法制化建設,提高倫理審查制度的法律層級,從而進一步明確法律責任,更好地保障受試者的合法權益。
因此,在借鑒國內外管理經驗的基礎上,原國家衛生計生委充分調研聽取各方面的意見,對《辦法(試行)》進行修訂,按照規章制定程序形成了《涉及人的生物醫學研究倫理審查辦法》(簡稱《11號令》)。《11號令》是為保護人的生命和健康,維護人的尊嚴,尊重和保護受試者的合法權益,規范涉及人的生物醫學研究倫理審查工作而制定。由國家衛生和計劃生育委員會于2016年10月12日作為“命令”發布,自2016年12月1日起施行。
《11號令》在內容方面進一步明確了醫療衛生倫理委員會的職責和任務;補充了倫理審查的原則、規程、標準和跟蹤審查的相關內容;進一步闡述了知情同意的基本內容和操作規程。
關于倫理審查的研究活動范圍,參照世界衛生組織《涉及人的生物醫學研究國際倫理準則》和世界醫學協會《赫爾辛基宣言》等文獻,在《辦法(試行)》基礎上補充了:采用流行病學、社會學、心理學等方法收集、記錄、使用、報告或儲存有關人的樣本、醫療記錄、行為等科學研究資料的活動。
《11號令》在監管方面明確了醫療衛生機構是涉及人的生物醫學研究倫理審查日常管理的責任主體;規定了縣級以上地方衛生計生行政部門對倫理委員會備案和倫理審查監管的職責和監督檢查的內容;明確了國家和省級醫學倫理專家委員會在監管工作中各自的職責任務。此外,《11號令》還補充了中醫藥管理部門對中醫藥研究項目倫理審查工作的監督管理職責以及中醫藥研究倫理委員會的職責任務。
今年3-4月,為保護人的生命和健康,維護人的尊嚴,尊重和保護受試者的合法權益,促進生命科學和醫學研究健康發展,國家衛健委將《涉及人的生物醫學研究倫理審查辦法》(國家衛生和計劃生育委員會令第11號)中行之有效的制度安排進行總結,并結合新的形勢和要求,會同有關部門起草了《涉及人的生命科學和醫學研究倫理審查辦法(征求意見稿)》,國家倫理審查監管工作持續改進中。
徐州健康熱線:0516-85707122









